ものはなぜ燃えるのか
質問
ものは、なぜ燃えるのですか。
回答
「ものが燃える」とは、可燃物と支燃物(酸素など、可燃物に結びついて可燃物を燃やすもの)が、着火源から熱をもらうことにより、高温で高速の発熱反応を起こし、可燃物と支燃物の化学エネルギーが熱と光のエネルギーに変換される現象を指します。
安定な物質が火気や電気火花などから熱をもらって高温になると、熱運動のエネルギーが増え、物質間で激しい衝突を起こしやすくなります。衝突の激しさがあるレベルに達すると、衝突した物質どうしが相互作用を起こし、物質を構成している原子どうしの結びつき(化学結合)に変化が生じます。それまで結びついていた同じ物質内の原子より、もっと結びつきやすい別の原子(例えば、コンロのガスやろうそくのロウの蒸気に含まれる水素原子と周囲空気中の酸素に含まれる酸素原子)との間で結合の組み換えが起こります。組み換え前より安定した強い結合ができると、組み換え前後の結合の強さの差に相当する化学エネルギーが物質から失われ、熱や光として外部に放出されます。 放出された熱エネルギーを、まだ燃えていない可燃物や支燃物が吸収して熱運動のエネルギーが増えると、さらに結合の組み換えが起こります。このようにして高温・高速で進行する、熱エネルギーの放出を伴う連続的な結合の組み換え過程が、「ものが燃える」という現象です。
ものが燃えるのは、突き詰めて言えば、物質を構成している原子間の化学結合の強さが、原子の組み合わせによって大きく異なる場合があるからです。
解説

なぜ燃えるかを知りたい場合、どういう時に燃えないかを想像してみることが、手がかりになります。
例(1):コンロの火をつける場合

例(2):ろうそくの燃え方 《 火も息をするのでしょうか? 》





まず考えてみて、仮説(仮の答え)を立ててから、実験映像をご覧ください。
火の三角形

ものが燃えるには、何が必要でしょうか?
ものが燃えるには、3つのアイテム「可燃物」「酸素」「熱」が必要です。
3つのアイテムが全部そろって、火の三角形が完成すると、ものが燃えます。

可燃物……コンロからでてくるガスや、車に入れるガソリン、ろうそく、バーベキューで使う炭など、燃えるもののことです。
酸素………空気の中に入っています。(→酸素がなくても燃える)
熱…………マッチやライターの炎、電熱線、レンズで集めた太陽の光などで熱を加えることにより、可燃物と酸素を高温にして結びつきやすくします。(→着火源)
エネルギーの山を越える

可燃物と酸素が熱を吸収して高温になると、熱運動のエネルギーが増え、化学結合の組み換えが起こりやすくなります。最初に結びついていた原子よりも新しく出会った原子の方が結びつき方が強いと、より安定な物質となって、物質が持つ化学エネルギーは減り、その分だけ熱が発生します。
温度がさらに上昇すると、可燃物と酸素が次々とエネルギーの山を越えて結びつくようになり、燃えはじめます。 可燃物と酸素が結びつくことにより、可燃物と酸素は減って、二酸化炭素(CO2)や水(H2O)など、燃える前より安定した強い化学結合を持つ燃焼生成物に変わります。燃えたあとに燃焼生成物が持っている化学エネルギーは、最初に可燃物と酸素が持っていた化学エネルギーより少なくなります。
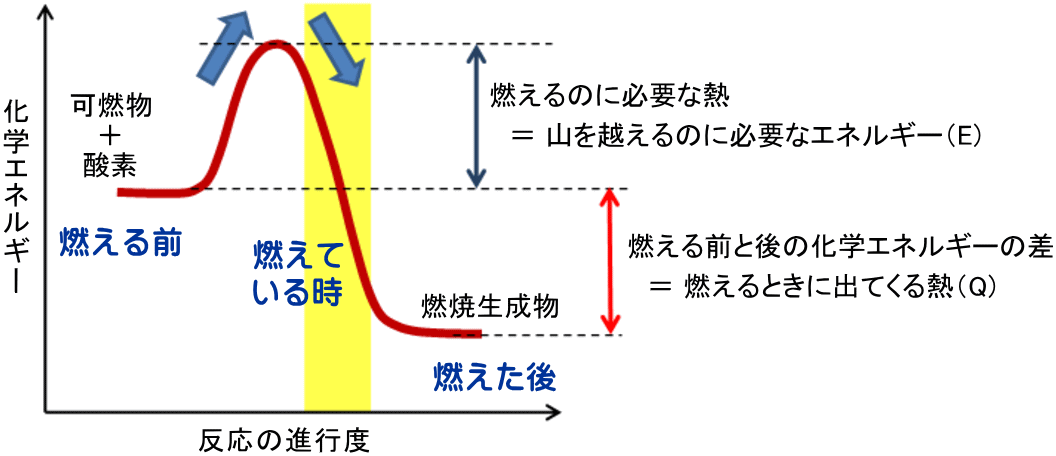
(※ 実際の可燃物と酸素の反応とはちがいます。)
燃えるのに必要な熱(E)より発生する熱(E+Q)の方が多いため、火の三角形の3つのアイテムの収支は次の式のようになります。
![]()
発生する熱は、可燃物と酸素だけでなく、空気中の窒素など、まわりにあるすべてのものに移ります。ものが燃えるかどうかは、火の三角形の3つのアイテムだけでなく、まわりにあるすべてのものと関わっています。
着火源
エネルギーの山を越えるのに必要な熱を可燃物と酸素に与えるものを、着火源と言います。(火の三角形の「熱」そのものを着火源と呼ぶこともあります。)着火源には、熱源や火気の他に、電気、静電気、衝撃火花、太陽光(鏡・レンズ)、雷など様々なものがあります。
 |
 |
 |
| コンロの火(熱) | コンセントの電気(漏電) | 静電気放電 |
 |
 |
 |
| 衝撃火花 | 凹面鏡による集光 | 落雷(かみなり) |
着火源の種類は違っても、ものを燃やすための役割は同じです。可燃物と酸素にエネルギーの山を越えさせること、これが着火源の役割です。 (ちなみに、私たちの体内にある唾液などの消化酵素と細胞内の呼吸酵素は、食物と酸素が炎を上げて燃えなくても結びつくことができるように、エネルギーの山を低くする役割をしています。)
https://www.nhk.or.jp/kokokoza/library/tv/seibutsukiso/archive/chapter006.html
(※ 日本放送協会ウェブサイトへリンク。アドレス確認日:2020年9月7日)
外部の着火源から熱をもらわなくても、可燃物と酸素が徐々に結びつくときに発生する熱や、可燃物が微生物によって分解されるときに発生する熱が、外部に逃げずに溜まりやすくなっていると、可燃物と酸素がエネルギーの山を越えて燃えだすことがあります。これを自然発火と言います。
→ 外部リンク【何もしていないのに燃え出す不思議「自然発火のはなし」】
https://www.jniosh.johas.go.jp/publication/mail_mag/2010/26-4.html
(※ 労働安全衛生総合研究所ウェブサイトへリンク。アドレス確認日:2020年9月7日)
なぜ燃え続けるのか? ~連鎖反応と連鎖担体~
可燃物と酸素がエネルギーの山を越えて結びついたときに発生した熱が、まだ燃えていない可燃物と酸素に伝わり、さらに次々と連続して、可燃物と酸素がエネルギーの山を越えて結びつく現象を、燃焼の「連鎖反応」と言います。可燃物も、酸素も、熱も、すべてこの連鎖反応を起こすために必要なのです。
連鎖反応が起こるためには、可燃物や酸素から発生する、「連鎖担体」と呼ばれる不安定な中間体(燃焼生成物になる前に一時的にできるもの)が、一定濃度以上、存在している必要があります。従って、熱の役割は、可燃物や酸素から連鎖担体を発生させること、とも言えます。
連鎖反応の過程を、最も単純な構造の可燃物である水素(H2)が酸素と結びついて燃える場合を例にとって紹介します。安定な水素分子(H2)と酸素分子(O2)に着火源から熱が与えられると、最初に、連鎖開始反応と呼ばれる遅い過程で、わずかの連鎖担体が発生します。
<連鎖開始反応の例>

水素に限らずコンロのガスやろうそくなど、多くの可燃物が酸素と結びついて燃えるときに、中心的な役割を担う連鎖担体は、水素原子(H)、酸素原子(O)、OHラジカル(OH)の3種類です。
連鎖開始反応によってわずかに発生した連鎖担体は、次に示す連鎖分岐反応で急速に増えます。
<連鎖分岐反応の例>

連鎖担体の数が増えも減りもしない連鎖成長反応も起こります。
<連鎖成長反応の例>

連鎖担体は連鎖停止反応によって失活し、比較的反応性が低い別の中間体や、燃焼生成物の水(H2O)などに変わります。 主要な連鎖停止反応は、第三体と呼ばれる、自分自身は反応しない安定な物質(窒素分子や水分子など)を含む、三重衝突による反応です。 第三体は、連鎖停止反応で出てくる熱を受け取ることによって、生成物を安定化し再び分解しないようにするはたらきをしています。 連鎖停止反応が起こるときには、大量の熱が発生します。
<連鎖停止反応の例>

ここで紹介した反応は、ものが燃えるときに起こっている反応のごく一部に過ぎません。コンロのガスやろうそくなどの可燃物が酸素と結びついて燃焼生成物ができるまでの間には、非常に多くの反応が関わっています。 「エネルギーの山を越える」では、山が1つだけの簡単な図を使って説明しましたが、ものが燃えるという現象は、実際には、様々な形状をした沢山のエネルギーの山や谷を経て進行します。(→参考文献)
燃焼の3要素

ものが燃えることを燃焼と言い、火の三角形は燃焼の3要素とも言います。 燃焼現象の中には、通常の燃焼と異なり、可燃物が空気中の酸素と結びつくのではなく別の支燃物と結びつくものがあります。 酸素以外の支燃物も「燃焼の3要素」に含めると、このようなタイプの燃焼も説明することができます。
<燃焼の3要素>
- 可燃物……燃えるもの
- 支燃物……可燃物に結びついて可燃物を燃やすもの
- 着火エネルギー……燃えるのに必要な熱
酸素がなくても燃える
可燃物に結びついて可燃物を燃やすはたらきをする「支燃物」は、空気中の酸素だけではありません。
<通常の燃焼> (例:コンロの火、ろうそく)
通常の燃焼では、空気中の酸素が支燃物です。

<酸素分子以外の酸化剤による燃焼> (例:花火、固体燃料ロケットの推進剤)
花火は、酸化剤(塩素酸カリウムなど)から発生する酸素が支燃物となります。

<自己反応性物質の燃焼> (例:無煙火薬、爆薬)
火薬や爆薬の多くは、1つの物質が可燃物と支燃物の両方を含んでいます。
自己反応性物質……他の支燃物(空気中の酸素など)がなくても、熱や衝撃を加えることにより燃焼・爆発する物質。
ダイナマイトの原料となるニトログリセリンなど。

さらに、酸素を含んでいなくても、酸化力が強く、可燃物と急速に結びついて大量の熱を放出する物質(たとえば塩素ガスやフッ素ガス)は、支燃物として作用します。
ものが燃えるときに起こる酸化反応は、酸素との反応だけではありません。
参考文献
三好 明:「燃焼化学の第一原理」、日本燃焼学会誌 第51巻157号(2009年)175-181
【外部リンク】https://chem.tut.ac.jp/keel/umc/archives/jcsj51_157_miyoshi.pdf
(※ 豊橋技術科学大学 環境・生命工学系ウェブサイトへリンク。アドレス確認日:2020年9月7日)












